Что надо сделать для ранней диагностики хронического миеломоноцитарного лейкоза? Пациенту, в первую очередь, необходимо записаться на консультацию к гематологу - онкологу.
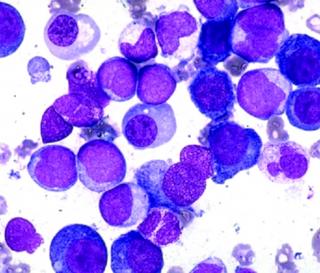
Первичный диагноз хронического миеломоноцитарного лейкоза ставят, если гематолог обнаруживает аномальные моноциты во время анализа крови. Затем пациента направляют на дообследование с помощью:
- анализа костного мозга - цитогенетический тест миелоидным секвенированием следующего поколения
- УЗИ лимфатических узлов
- УЗИ селезенки
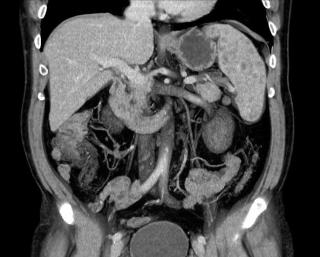
- МРТ брюшной полости
- ПЭТ-КТ.
Хронический миеломоноцитарный лейкоз (ХММЛ или CMML) - редкий тип рака крови. При ХММЛ в крови образуется слишком много моноцитов. Моноциты - это разновидность белых кровяных телец. Всемирная организация здравоохранения (ВОЗ) включила хронический миеломоноцитарный лейкоз в группу рака крови, называемую миелопролиферативными и миелодиспластическими заболеваниями. ХММЛ расценивается как отдельное состояние с различными вариантами лечения, поскольку у больных могут быть признаки как миелопролиферативных, так и миелодиспластических расстройств.
Костный мозг - это мягкая внутренняя часть костей, из которой состоят клетки крови. Все клетки крови берут начало от клеток одного и того же типа, называемых стволовыми клетками. Стволовая клетка производит незрелые клетки крови. Эти незрелые клетки проходят различные стадии развития, прежде чем стать полностью развитыми клетками крови. Костный мозг производит различные типы клеток крови, в том числе:
- красные кровяные тельца, которые переносят кислород по телу
- лейкоциты для борьбы с инфекцией
- тромбоциты, чтобы помочь свертыванию крови.
Что такое миелопролиферативные и миелодиспластические заболевания
Миелопролиферативное заболевание - это состояние, при котором вырабатывается слишком много клеток крови. Миелодиспластическое заболевание - это состояние, когда вырабатываемые клетки крови являются аномальными и не полностью созрели. В действительности эти два расстройства часто пересекаются, поэтому ВОЗ объединила их в одну категорию.
Моноциты являются частью иммунной системы и помогают организму бороться с инфекцией, однако при раке крови их слишком много, и они недостаточно развиты, чтобы работать должным образом. Костному мозгу в таком состоянии трудно производить другие клетки крови, такие как:
- красные кровяные тельца
- тромбоциты
- другие лейкоциты
- потому, что моноциты занимают много места в костном мозге.
Что происходит в костном мозге при хроническом миеломоноцитарном лейкозе
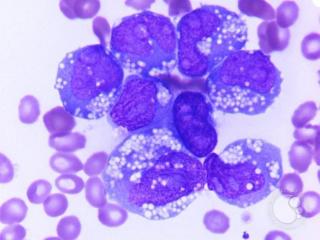
Белые кровяные тельца, называемые моноцитами, помогают организму бороться с инфекцией. При хроническом миеломоноцитарном лейкозе костный мозг производит аномальные моноциты. Они не полностью развиты и не могут нормально функционировать. Также иногда наблюдается увеличение незрелых клеток, называемых бластными клетками. Эти аномальные клетки крови либо остаются в костном мозге, либо разрушаются, прежде чем попадут в кровоток. По мере развития лейкоза костный мозг наполняется аномальными моноцитами, и затем эти аномальные клетки крови попадают в кровоток. Поскольку костный мозг полон аномальных клеток, он не может производить достаточно других типов клеток крови. Низкое количество нормальных клеток крови в кровотоке в конечном итоге вызывает симптомы лейкоза.
Причины хронического миеломоноцитарного лейкоза
Онкологи не знают причины большинства случаев хронического миеломоноцитарного лейкоза, но есть некоторые факторы риска, которые могут
увеличить риск его развития. Шансы развития ХММЛ увеличивается с возрастом. Средний возраст постановки диагноза составляет от 71 до 74 лет, и чаще встречается у мужчин, чем у женщин. Иногда причиной лейкоза является лучевая терапия или химиотерапевтическое лечение рака. Это называется вторичным или связанным с лечением хроническим миеломоноцитарным лейкозом.
Около половины всех людей с ХММЛ (около 50%) имеют изменение в гене, называемом TET2. Ген TET2 вырабатывает белок, который контролирует количество моноцитов в стволовых клетках. До 30 из 100 пациентов имеют изменение в гене, называемом RAS. Изменение заставляет клетки бесконтрольно размножаться. Есть и другие гены, изменения которых могут привести к ХММЛ, к ним относятся:
- ASXL1
- SRSF2.
Многие больные с хроническим миеломоноцитарным лейкозом имеют более одного изменения гена.
Симптомы хронического миеломоноцитарного лейкоза
Хронический миеломоноцитарный лейкоз обычно развивается медленно и сначала не вызывает симптомов. На более поздних этапах признаки могут включать:
- усталость и иногда одышка из-за низкого количества эритроцитов (анемия) инфекции, которые не проходят
- кровотечение (например, носовое кровотечение) или легкое образование синяков из-за низкого количества тромбоцитов
- дискомфорт в животе от опухоли селезенки
- кожные высыпания
- одышка из-за жидкости в плевральном выпоте.
Типы хронического миеломоноцитарного лейкоза
Всемирная организация здравоохранения разделила хронический миеломоноцитарный лейкоз на 3 типа. Их называют типом 0, типом 1 и типом 2. Тип лейкоза определяют по количеству аномальных миелоидных клеток (бластов) в крови и образцах костного мозга.
Врачи описывают количество бластных клеток в процентах. Это количество бластных клеток на каждые 100 лейкоцитов.
ХММЛ типа 0 означает, что у пациента менее 2% бластных клеток в крови и менее 5% бластных клеток в костном мозге.
ХММЛ типа 1 означает, что у пациента 2–4% бластных клеток в крови или 5–9% бластов в костном мозге. У некоторых пациентов наблюдается и то, и другое.
ХММЛ типа 2 означает, что у пациента 5-19% бластных клеток в крови и 10-19% в костном мозге.
Наличие стержней Ауэра в образцах означает, что у пациента ХММЛ типа 2. Стержни Ауэра - это материал внутри ячеек ХММЛ, который выглядит как длинные иглы и видны только внутри аномальных клеток.
Группы риска
Врачи используют классификацию пациентов по группам риска, чтобы попытаться предсказать шансы на излечения онкобольного . Факторы влияющие на уровень риска включают:
- тип хронического миеломоноцитарного лейкоза
- количество лейкоцитов
- любые генетические изменения в клетках ХММЛ
- уровень количества эритроцитов.
Хронический миеломоноцитарный лейкоз может перерасти в острый миелоидный лейкоз, если количество бластных клеток в крови превышает 20%. Врачи называют это перерождением. По статистике трансформация происходит у 15–30 из каждых 100 онкобольных.
Диагностика хронического миеломоноцитарного лейкоза
Первичный диагноз хронического миеломоноцитарного лейкоза ставят, если гематолог обнаруживает аномальные моноциты во время анализа крови. Затем пациента направляют на дообследование с помощью:
- анализа костного мозга - цитогенетический тест миелоидным секвенированием следующего поколения
- УЗИ лимфатических узлов
- УЗИ селезенки
- МРТ брюшной полости
- ПЭТ-КТ.
Лечение хронического миеломоноцитарного лейкоза
Тип необходимого лечения зависит от следующих факторов:
- тип ХММЛ
- наличия симптомов
- возраст
- есть ли у вас какие-либо другие заболевания.
Единственный способ вылечить хронический миеломоноцитарный лейкоз - это трансплантация стволовых клеток. Это интенсивное лечение, сопряженное с множеством рисков, поэтому, к сожалению, оно подходит не всем.
Большинству онкобольных в какой-то момент требуется поддерживающее лечение в зависимости от типа имеющихся симптомов.
Возможно, пациенту сделают переливание крови, если наблюдается низкий уровень эритроцитов. При низком уровне тромбоцитов, может потребоваться переливание тромбоцитов, особенно если пациент испытывает какие-либо симптомы кровотечения.
Частые переливания крови могут вызвать накопления железа в организме, что может повредить сердце и печень, поэтому пациенту, возможно, придется принимать лекарства, чтобы избавиться от лишнего железа.
Факторы роста - это лекарства, которые стимулируют костный мозг производить больше клеток крови. Эритропоэтин - фактор роста, увеличивающий количество красных кровяных телец. Г-КСФ - это фактор роста, увеличивающий количество лейкоцитов. Оба эти препарата вводятся в виде инъекций непосредственно под кожу чтобы стимулировать нужное количество компонентов крови.
Онкобольному может потребоваться прием антибиотиков для лечения инфекции, а иногда и для предотвращения инфекции.
Химиотерапия при хроническом миеломоноцитарном лейкозе
В химиотерапии используются препараты, убивающие клетки (цитотоксические), для уничтожения аномальных клеток. Лекарства действуют, нарушая рост клеток и не давая им делиться. Тип химиотерапии зависит от вида онкологии и общего состояния здоровья. Первая химиотерапия может включать такие препараты, как азацитидином, гидроксикарбамидом или цитарабином в низких дозах.
Азацитидин - это лекарство, называемое гипометилирующим агентом, которое работает, отключая белок, называемый ДНК-метилтрансферазой, что включает гены, которые останавливают рост и деление раковых клеток. Такая терапия уменьшает количество аномальных клеток крови и помогает контролировать рост клеток.
Гидроксикарбамид (гидроксимочевина)
Онкобольному может быть назначен гидроксикарбамид, чтобы контролировать высокое количество лейкоцитов. Гидроксикарбамид является одним из группы химиотерапевтических препаратов, известных как антиметаболиты. Эти препараты останавливают производство и восстановление ДНК клеток. Раковые клетки должны производить и восстанавливать ДНК, чтобы расти и размножаться.
Если больной не может принимать гидроксикарбамид, ему могут быть назначены низкие дозы цитарабина, который убивает злокачественные клетки, не позволяя им создавать и восстанавливать ДНК, необходимую для роста и размножения.
Трансплантация донорских стволовых клеток
Трансплантация донорских стволовых клеток обычно подходит только пациентам, которые:
- имеют достаточно молодой возраст
- хорошее состояния здоровья
- имеют подходящего донора.
Процедура трансплантации донорских стволовых клеток проходит в несколько этапов интенсивная терапия перед пересадкой, трансплантация и поддерживающая терапия после пересадке. Перед трансплантацией стволовых клеток онкобольному может быть назначена интенсивная химиотерапия с целью контролировать заболевание. Она похожа на химиотерапию, которую проводят при остром лейкозе, на базе препаратов:
- флударабин, цитарабин и идарубицин (FLAG - Ida)
- цитарабин и даунорубицин (DA).
Лучевая терапия, химиотерапия и таргетные препараты, которые назначаются перед пересадкой, имеют хорошие шансы убить злокачественные клетки, но он также убивают стволовые клетки в костном мозге.
Некоторым больным, перенесшим донорскую трансплантацию, может быть сделана мини-трансплантация, так называемая трансплантация кондиционирования с пониженной интенсивностью (RIC). При этой процедуре применяется более низкие дозы химиотерапии, чем при традиционной трансплантации стволовых клеток, и она может лучше подходить онкобольным старше 50 лет, которые не подходят для традиционной трансплантации или недостаточно хорошо себя чувствуют.
Для пересадки пациенту необходимо донор стволовых клеток. Наиболее подходящим донором обычно является близкий родственник, например, брат или сестра. Чтобы донорские стволовые клетки начали производить новые клетки крови, требуется от нескольких дней до нескольких недель. В это время пациенту потребуются переливания крови и тромбоцитов.
Болезнь трансплантат против хозяина (РТПХ) может быть серьезным возможным осложнением трансплантации стволовых клеток или костного мозга от другого человека.
Ведущие врачи в СПб







Список научной литературы:
- Л.А.Хачатрян, Е.В.Самочатова, М.А.Масчан, Д.Д.Байдильдина, Г.Г.Солопова, А.А.Масчан. «Результаты терапии ювенильного миеломоноцитарного лейкоза у детей». Сборник материалов XV Российского национального конгресса «Человек и лекарство»,Москва , 14-18 апреля 2008: С.423
- Лубкова, О.Н. Экспрессия VCAM-1 на стромальных клетках из костного мозга больных миелодиспластическими синдромами / О.Н. Лубкова, Н.В. Цветаева, К.С. Момотюк, В.М. Белкин, Т.Е. Манакова // Бюллетень экспериментальной биологии и медицины. - 2011. -N 1.-е. 17-20.
- Абдулкадыров, K.M. Клиническая гематология, справочник / K.M. Абдулкадыров. - Москва - Санкт-Петербург, 2006. - 447 с.
- Головской Б. В., Баев В. М., Юдина О.Н. Синдром повышенной вязкости крови у больных хроническими миело и лимфолейкозами //Гематология и трансфузиология. - 1997. - №6 - С. 10-12.
- Тиссен Т.П. Магнитно-резонансная ангиография в диагностике сосудистой патологии головного и спинного мозга / Тиссен Т.П., Белова Т.В., Климчук О.В., Шевелев И.Н. // Нейрохирургия. - 2002. - № 3. - С. 6-12.
- Вольтер С. А. Ультразвуковая диагностика: Нормативные материалы и методические рекомендации / Больтер С. А. М.: Медицина, 1990. - 567 с.
Что надо сделать для ранней диагностики острого лимфобластного лейкоза? Пациенту, в первую очередь, необходимо записаться на консультацию к терапевту. После первичного приема врач может назначить дополнительно обследования: Анализы крови на острый лимфобластный лейкоз (ОЛЛ) Исследование костного мозга Люмбальная пункция Рентген грудной клетки КТ шеи КТ груди КТ брюшной полости КТ малого таза МРТ центральной нервной системы УЗИ брюшной полости УЗИ лимфатических узлов Анализ крови или слюны для проверки типа ткани.
Что надо сделать для ранней диагностики острого лимфобластного лейкоза? Пациенту, в первую очередь, необходимо записаться на консультацию к терапевту. После первичного приема врач может назначить дополнительно обследования: Анализы крови на острый лимфобластный лейкоз (ОЛЛ) Исследование костного мозга Люмбальная пункция Рентген грудной клетки КТ шеи КТ груди КТ брюшной полости КТ малого таза МРТ центральной нервной системы УЗИ брюшной полости УЗИ лимфатических узлов Анализ крови или слюны для проверки типа ткани.
Что надо сделать для ранней диагностики хронического миелоидного лейкоза? Пациенту, в первую очередь, необходимо записаться на консультацию к гематологу или онкологу. После первичного приема врач может назначить дополнительно обследования: общий анализ крови биопсия костного мозга КТ легких МРТ брюшной полости УЗИ лимфатических узлов ПЭТ-КТ.
Что надо сделать для ранней диагностики хронического миелоидного лейкоза? Пациенту, в первую очередь, необходимо записаться на консультацию к гематологу или онкологу. После первичного приема врач может назначить дополнительно обследования: общий анализ крови биопсия костного мозга КТ легких МРТ брюшной полости УЗИ лимфатических узлов ПЭТ-КТ.
МРТ брюшной полости, наряду с томографией органов малого таза, требует подготовки пациента перед исследованием. От качества подготовительных мероприятий во многом зависит информативность и результативность томографии области живота.
МРТ брюшной полости, наряду с томографией органов малого таза, требует подготовки пациента перед исследованием. От качества подготовительных мероприятий во многом зависит информативность и результативность томографии области живота.
 Общегородской центр
Общегородской центр