Что надо сделать для ранней диагностики саркомы мягких тканей? Пациенту, в первую очередь, необходимо записаться на консультацию к онкологу. После первичного приема врач может назначить дополнительные обследования:
- УЗИ мягких тканей
- МРТ
- Пункционную биопсию
- Хирургическую биопсию
- Тесты на генные изменения
- Рентген
- Компьютерную томографию.
Что такое саркомы мягких тканей
Саркомы мягких тканей — это злокачественные новообразования, которые развиваются в соединительных и поддерживающих тканях, включая: мышцы, кровеносные сосуды, глубокие ткани кожи, нервы, сухожилия и связки. Вместе эти ткани известны как соединительные ткани. Они соединяют, поддерживают или окружают другие структуры или органы тела. Кости также являются опорной тканью. Существуют различные типы саркомы, которые поражают кости.
Саркомы мягких тканей чаще всего встречаются у пожилых людей. Но по сравнению с большинством других видов рака, они довольно часто встречается у молодых людей.
Где возникают саркомы мягких тканей?
Мягкие ткани есть во всех частях тела. Таким образом, саркомы мягких тканей могут развиваться и расти практически в любом месте. Если саркому не лечить, клетки продолжают делиться, и саркома будет увеличиваться в размерах. Рост саркомы вызывает уплотнение в мягких тканях. Это может вызвать давление на любые ткани или органы тела поблизости.
Клетки саркомы из исходной области могут отделиться. Если злокачественные клетки попадают в кровоток, они могут распространяться на другие части тела. Затем эти клетки могут образовывать новые области саркомы, которые известны как вторичный рак или метастазы. Саркомы чаще всего распространяются на легкие и кости.
Виды сарком мягких тканей
Существует много различных типов сарком мягких тканей:
Лейомиосаркома
Лейомиосаркома является наиболее распространенным типом саркомы мягких тканей у взрослых. Это вип гладкомышечной опухоли. Эти мышцы образуют стенки матки, пищеварительной системы и кровеносных сосудов. Лейомиосаркомы могут расти в:
- брюшной полости
- забрюшинном пространстве
- крупных кровеносных сосудах
- матке
- коже
- конечностях.
Воспалительная лейомиосаркома
Другой тип рака гладких мышц у взрослых — воспалительная лейомиосаркома. Этот вид саркомы имеет тенденцию к росту в следующих тканях:
- глубоких мягких тканях голени
- мягких тканях груди
- забрюшинном пространстве.
Липосаркома
Липосаркомы развиваются из жировой ткани и могут расти в любом месте тела. Наиболее частыми локализациями являются бедра и забрюшинное пространство. Обычно они проявляются в виде мягких комочков. Около 20% сарком мягких тканей у взрослых являются липосаркомами. Видами злокачественных опухолей, которые растут из жировой ткани, являются:
- хорошо дифференцированная липосаркома
- дедифференцированная липосаркома
- миксоидная липосаркома
- плеоморфная липосаркома.
Фибросаркомы
Фибросаркомы представляют собой тип фибробластной опухоли. Они растут из клеток фиброзной ткани. Фибросаркомы встречаются редко и составляют примерно 1% сарком мягких тканей. Они могут расти в следующих локациях:
- глубоких тканях рук или ног
- ткани живота
- мягких тканях головы и шеи.
Другие виды злокачественных образований тканей включают:
- солитарную фиброзную опухоль
- миксофибросаркому
- фибромиксоидную саркому низкой степени злокачественности
- склерозирующую эпителиоидную фибросаркому.
Рабдомиосаркомы
Рабдомиосаркомы развиваются из клеток скелетных мышц. Есть несколько типов рабдомиосарком:
- эмбриональные рабдомиосаркомы (чаще у детей, редко у подростков и взрослых)
- альвеолярные рабдомиосаркомы (чаще у подростков и взрослых)
- плеоморфная рабдомиосаркома (чаще всего у взрослых)
- веретеноклеточная или склерозирующая рабдомиосаркома
- эктомезенхимома.
Синовиальные саркомы
Синовиальные саркомы представляют собой тип опухоли неопределенной дифференцировки. Это означает, что исходная клетка неизвестна. Эти саркомы состоят из клеток, которые не похожи ни на какой конкретный тип мягких тканей, так что онкологам трудно определить, где начался рак. Синовиальные саркомы чаще всего растут вокруг коленных, голеностопных, тазобедренных или плечевых суставов. Хотя они называются синовиальными саркомами, они не начинаются в ткани, которая выстилает суставы (синовиальная ткань). Их можно найти в областях, где нет синовиальной ткани, например, мягкие ткани головы и шеи. Эти саркомы обычно проявляются в виде твердых уплотнений.
Другие виды опухолей неясного происхождения включают:
- эпителиоидную саркому
- альвеолярную саркому мягких тканей
- светлоклеточную саркому
- внескелетную миксоидную хондросаркому
- десмопластическаую мелкокруглоклеточную опухоль
- рабдоидную опухоль
- периваскулярную эпителиоидную опухоль.
Эпителиоидная гемангиоэндотелиома
Эти опухоли начинаются в мягких тканях или внутренних органах, таких как легкие.
Злокачественные опухоли оболочек периферических нервов
Злокачественные опухоли оболочек периферических нервов являются разновидностью опухолей оболочек периферических нервов. Эти виды рака начинаются в оболочке нерва, покрывающего периферические нервы, которые посылают сообщения между головным и спинным мозгом и остальной частью тела. Наиболее распространенными локациями опухоли являются ноги и забрюшинное пространство.
Другие виды опухолей оболочек периферических нервов включают:
- меланотическую злокачественную опухоль оболочки нерва
- зернистоклеточную опухоль
- периневриому.
Желудочно-кишечные стромальные опухоли
Желудочно-кишечные стромальные опухоли - это редкий тип саркомы, обнаруживаемый в пищеварительной системе. Они могут развиваться в любой части желудочно-кишечного тракта, но наиболее распространенными локациями являются желудок и тонкая кишка.
Фолликулярная дендритно-клеточная саркома
Фолликулярная дендритно-клеточная саркома (саркома ФДК) является очень редким типом саркомы, которая развивается из специализированных клеток в лимфатических узлах.
Фиброматоз
Фиброматоз не является раком и развивается из глубоких соединительных тканей. Он не распространяется по телу, но может проникать в близлежащие ткани. Его также называют агрессивным фиброматозом или десмоидной опухолью. Фиброматоз встречается редко. Он может начаться в любом месте тела, но чаще встречается в следующих локациях:
- руках или ногах
- брюшной стенке
- ткани, которая прикрепляет тонкую и толстую кишку к задней стенке живота (брыжейке).
Симптомы саркомы
Симптомы саркомы мягких тканей будут различаться в зависимости от размера опухоли и ее локализации в организме. На ранних стадиях саркомы мягких тканей обычно не вызывают симптомов. Поскольку саркомы могут расти в любом месте тела, на поздних стадиях онкологии симптомы будут зависеть от того, где находится новообразование, и могут включать:
- уплотнение, которое сначала безболезненное
- уплотнение, растущие в размерах
- болезненность, когда шишка растет и давит на нервы и мышцы.
Уплотнение, скорее всего, является саркомой, если оно:
- более 5 см или становится больше
- находится глубоко в тканях
- болезненно при прикосновении
- вернулось после предыдущей операции по удалению саркомы.
Риски сарком мягких тканей
Риск развития рака мягких тканей зависит от многих факторов, в том числе:
- возраста
- генетики
- образа жизни
- экологических факторов.
Саркомы мягких тканей могут развиваться у людей любого возраста, но, как и в случае большинства видов рака, риск увеличивается с возрастом. Около 40% сарком по статистике диагностируются у людей в возрасте 65 лет и старше. Менее чем у 1% людей, прошедших лучевую терапию по поводу других видов рака, спустя годы может развиться саркома в области лечения. Это связано с тем, что облучение может воздействовать на здоровые ткани в обрабатываемой области. Увеличение этого риска зависит от следующих факторов:
- возраста человека
- расположения рака
- дозы лучевой терапии.
Больные, получившие высокие дозы лучевой терапии в детстве, имеют наибольший риск возникновения сарком. Сочетание химиотерапии с лучевой терапией может еще больше увеличить риск. У взрослых врачи связывают саркомы, вызванные предшествующей лучевой терапией, с лечением таких видов рака, как:
- рак молочной железы
- лимфома
- рак матки
- рак простаты
- рак головы и шеи
- рак кишечника
- герминогенные опухоли.
У детей риск лучевой сарком связан с предшествующим лечением лучевой терапией по поводу:
- ретинобластомы
- саркомы Юинга
- рабдомиосаркомы
- лимфомы Ходжкина
- опухоли головного мозга
- опухоли Вильмса.
Ионизирующее излучение в окружающей среде также может увеличить риск развития саркомы.
Считается, что некоторые химические вещества, возможно, увеличивают риск некоторых типов саркомы. Это может быть в ситуациях, когда люди подвергались воздействию высоких уровней на своей работе в течение многих лет. Следующие химические вещества имеют ограниченные доказательства того, что они вызывают саркому мягких тканей:
- радиоактивные йоды, включая йод-131
- полихлорфенолы
- 2,3,7,8-тетрахлордибензо-пара-диоксин.
Некоторые типы редких генетических состояний могут увеличить риск развития злокачественной опухоли мягких тканей. Нейрофиброматоз - это генетическое заболевание, которое увеличивает риск получения редкого типа саркомы, называемой злокачественной опухолью оболочки периферических нервов.
Синдром Ли Фраумени - это генетический синдром, возникающий из-за имутации в гене TP53, которое останавливает рост опухоли. Его иногда называют синдромом семейного рака. Семьи с синдромом Ли Фраумени имеют более высокий риск развития саркомы мягких тканей.
Дети, у которых была ретинобластома, имеют повышенный риск развития саркомы мягких тканей в будущем. Наиболее распространенные типы:
- лейомиосаркома
- фибросаркома
- рабдомиосаркома.
Лучевая терапия, применяемая для лечения ретинобластомы, является частью повышенного риска. Эти дети также имеют повышенный риск развития рака кости, называемого остеосаркомой.
Инфекция, называемая вирусом Эпштейна-Барра (EBV), связана с лейомиосаркомой.
Лучевая терапия и хирургическое вмешательство при раке молочной железы могут вызвать долговременный отек (лимфедему) руки. Лучевая терапия или хирургическое вмешательство в области таза или гениталий может вызвать отек ноги. У женщин с хроническим лимфедемой рук после удаления молочной железы (мастэктомии) может развиться ангиосаркома. Это очень редкое заболевание, также известное как синдром Стюарта-Тревеса. Реже ангиосаркома может возникать в ноге у людей с хроническим лимфедемой ноги.
Саркома Юинга более вероятна у детей, рожденных с:
- грыжей пупка (врожденная пупочная грыжа)
- грыжей в верхней части ноги (паховая грыжа).
Пупочная грыжа возникает из-за слабости мышц вокруг пупка. Паховая грыжа – это слабость мышц в паховой области, однако пока неясно, почему грыжи увеличивают риск саркомы.
Женщины с очень избыточным весом могут иметь более высокий риск развития саркомы матки.
Иногда люди думают, что травма вызвала рак. Нет никаких доказательств того, что любая травма может вызвать саркому, однако она может привлечь внимание к уже существующей саркоме, когда человеку сделали рентген, КТ или МРТ.
Диагностика саркомы мягких тканей
Дифференциальная диагностика и лечение саркомы требует комплексного обследования. Расширенный перечень исследований позволяет безопасно планировать операции, лучевую терапию, химиотерапию и вовремя замечать осложнения. Анализы крови и мочи помогают контролировать работу костного мозга, печени, почек и свёртывающей системы в условиях нагрузки лекарствами и облучением. Визуализирующие методы, такие как рентгенография, КТ, МРТ, ПЭТ-КТ, дают представление о размерах первичного очага, наличии метастазов и динамике на фоне терапии. Морфологические, иммуногистохимические и молекулярно-генетические тесты уточняют подтип саркомы и подсказывают, какие схемы лечения будут наиболее результативны.
- Общий и биохимический анализ крови, а также коагулограмма назначаются перед началом лечения саркомы, в том числе перед операцией, химиотерапией и лучевой терапией, затем выполняются в процессе и на этапах наблюдения. По данным анализов оцениваются уровень гемоглобина, лейкоцитов, тромбоцитов, показатели свёртывания, функции печени и почек, что позволяет безопасно планировать наркоз, подбирать дозы цитостатиков и контролировать токсичность. При выявлении отклонений схема терапии корректируется, при выраженной анемии или тромбоцитопении рассматриваются трансфузии и дополнительная поддержка.
- Общий анализ мочи используется до начала лечения и периодически в ходе комбинированной терапии для оценки состояния мочевыделительной системы, особенно при применении нефротоксичных препаратов или облучении тазовой области. Исследование помогает вовремя заметить признаки воспаления, протеинурии, гематурии, что может указывать на поражение почек или мочевых путей. При изменениях в анализе мочи онколог корректирует схему, режим гидратации и объём наблюдения.
- ЭКГ выполняется перед оперативным вмешательством, курсами химиотерапии и лучевой терапией, а затем повторяется при наличии жалоб или применении кардиотоксичных препаратов. По результатам оценивается ритм, проводимость, наличие ишемических изменений, что влияет на выбор анестезии и возможность назначения антрациклинов. При выявлении нарушений пациент дополнительно направляется к кардиологу, чтобы снизить риск осложнений во время лечения саркомы.
- УЗИ сердца назначается при подготовке к химиотерапии с антрациклинами и другими потенциально кардиотоксичными средствами, а также при длительных программах лечения высокозлокачественных сарком. Исследование позволяет оценить фракцию выброса, состояние клапанного аппарата, признаки перегрузки или кардиомиопатии. В динамике эхокардиография используется для своевременного выявления снижения сократимости и решения вопроса о смене схемы или снижении доз.
- МРТ мягких тканей выполняется до лечения для точного определения размеров опухоли, вовлечения мышц, фасций, суставов, сосудисто-нервных пучков, а также после неоадъювантной химиотерапии или лучевой терапии для оценки ответа. В послеоперационном периоде МРТ используется для раннего выявления локальных рецидивов, особенно при мягкотканных саркомах конечностей, тазовой области и паравертебральных локализациях. Высокая контрастность мягких тканей делает данное исследование основным методом локальной оценки.
- КТ брюшной полости и КТ забрюшинного пространства применяется при подозрении на метастатическое распространение саркомы, при забрюшинных и висцеральных локализациях, а также при контроле динамики на фоне системной терапии. Исследование позволяет оценить размер и структуру очагов, связь с сосудами и окружающими органами, наличие плеврального или перитонеального выпота. В дальнейшем КТ используется на этапах наблюдения для своевременного выявления новых метастазов или прогрессирования уже известных.
- ПЭТ-КТ всего тела назначается при высокозлокачественных саркомах, неясных очагах на КТ или МРТ, а также при планировании объёма лучевой терапии и оценке ответа на системное лечение. Комбинация метаболической информации и анатомического изображения помогает уточнить распространённость процесса, отличить активную опухолевую ткань от рубца или фиброза, что особенно важно после операций и облучения. В динамике ПЭТ-КТ позволяет оценить эффективность химиотерапии и таргетной терапии при GIST и других подтипах.
- Морфологический и иммуногистохимический пересмотр опухолевой ткани выполняется до начала лечения в специализированном центре, а при рецидивах и прогрессировании может повторяться по новому биоптийному материалу. Анализ срезов, расширенные панели маркёров и уточнение подтипа саркомы позволяют скорректировать выбор схем химиотерапии, объём лучевой терапии и показания к таргетному лечению. При изменении морфологической картины в процессе лечения клинический онколог получает более точные данные о биологии опухоли.
Существуют генетические тесты, которые смотрят на хромосомы и гены в раковых клетках. Их называют цитогенетическими тестами. Эти тесты проверяют, есть ли какие-либо мутации в клетках, что позволяет определить тип злокачественных клеток. Дело в том, что существует много различных типов сарком мягких тканей. Онкологам иногда бывает трудно отличить одно от другого, но врачи знают, что некоторые гены связаны с определенными типами саркомы мягких тканей:
- Синдром Ли-Фраумени вызван изменениями в гене-супрессоре опухоли TP53. Он связан с такими саркомами, как рабдомиосаркома, лейомиосаркома и липосаркома.
- Нейрофиброматоз 1 с мутациями в гене NF1 связан со злокачественной опухолью оболочек периферических нервов.
- Ретинобластома с изменениями в гене RB1 связана с лейомиосаркомой.
Подробные тесты генов в клетках саркомы могут помочь точно определить вид саркомы.
Какие врачи
- Онколог координирует лечение сарком, формирует общий план комбинированной терапии и задаёт последовательность этапов. В обязанности входит анализ гистологии и молекулярных маркеров, оценка стадии, стратификация по риску и выбор, в каком порядке использовать операцию, лучевую терапию и системные методы. Клинический онколог объясняет пациенту цели каждого этапа, согласует лечение с узкими специалистами, контролирует переносимость и своевременную коррекцию схем, принимает решения о переходе на следующие линии терапии при прогрессировании.
- Хирург-онколог отвечает за радикальное удаление сарком мягких тканей, забрюшинных опухолей, дерматофибросаркомы протуберанс, солитарной фиброзной опухоли и других образований, где ключевую роль играет адекватный краевой отступ. Специалист планирует объём операции по данным МРТ, КТ, ПЭТ-КТ, определяет необходимость комбинированных резекций соседних органов и реконструктивных вмешательств. Во время операции хирург ориентируется на задачи онкологического радикализма, а после вмешательства взаимодействует с радиотерапевтом и клиническим онкологом по вопросу адъювантного лечения.
- Радиотерапевт отвечает за все этапы лучевого лечения при саркомах мягких тканей, костных опухолях, солитарных фиброзных опухолях, саркоме Капоши и ряде других форм. Специалист определяет объём мишени, рисковые зоны, выбирает технику облучения (3D-конформная, IMRT, VMAT, стереотаксическая методика), рассчитывает дозу и режим фракционирования. Радиотерапевт контролирует острые лучевые реакции, при необходимости меняет график сеансов, тесно взаимодействует с клиническим онкологом, хирургами и реабилитологом.
- Онколог-химиотерапевт или онкогематолог ведёт системное лечение высокозлокачественных сарком, агрессивных мягкотканных форм. Специалист подбирает химиотерапевтические схемы, рассчитывает дозы с учётом функции печени и почек, контролирует токсичность, при необходимости изменяет режим. В задачи входит коррекция побочных эффектов, назначение факторной поддержки, согласование сроков курсов с операциями и облучением, чтобы не снижать общую эффективность программы.
- Специалист по таргетной терапии и иммуноонкологическим методам особенно важен при GIST, дерматофибросаркоме протуберанс с транслокацией COL1A1–PDGFB, отдельных вариантах ангиосарком и эпителиоидной саркомы. Такой онколог ориентируется в мутационном профиле опухоли, назначает ингибиторы тирозинкиназ, антиангиогенные препараты, современные иммунопрепараты, контролирует длительность приёма и переносимость. При прогрессировании по данным визуализирующих методов специалист решает вопрос о смене линии, временной отмене или комбинировании с локальными методами лечения.
- Патоморфолог играет ключевую роль с момента первичной биопсии саркомы и до анализа операционного материала. Специалист определяет тип саркомы, степень злокачественности, маргинальный статус, оценивает процент некроза после неоадъювантной химиотерапии или лучевого этапа. Дополнительно используются иммуногистохимические и молекулярные исследования, позволяющие уточнить диагноз, выявить мишени для таргетной терапии и уточнить прогноз, на основании чего клинический онколог и химиотерапевт корректируют стратегию.
- Реабилитолог необходим при лечении сарком конечностей, забрюшинных опухолей, MPNST и других форм, где затрагиваются мышцы, нервы и суставы. Специалист подбирает индивидуальную программу восстановления после обширных операций и лучевой терапии, контролирует объём и темп физических нагрузок, обучает безопасным движениям и правильному использованию ортезов, костылей, протезов. Целью служит сохранение максимально возможной функции конечности, предотвращение контрактур, лимфедемы, выраженной мышечной атрофии.
- Психоонколог или клинический психолог помогает пациентам с саркомами справляться с диагнозом, длительным комбинированным лечением, возможной инвалидизацией и страхом рецидива. Специалист проводит индивидуальные консультации, обучает методам саморегуляции, работает с тревогой, депрессией, нарушениями сна, при необходимости направляет к психиатру для подбора медикаментозной поддержки. Важным направлением остаётся помощь семье, чтобы близкие лучше понимали эмоциональные реакции пациента и не усиливали стресс непосильными ожиданиями.
- Специалист по паллиативной помощи подключается при запущенных и резистентных формах сарком, когда основная задача смещается в сторону контроля симптомов и поддержания качества жизни. Команда подбирает оптимальную анальгетическую терапию, противорвотные и противозудные средства, корректирует дыхательную недостаточность, расстройства питания, отёки. Паллиативная служба помогает организовать домашний уход, обучает родственников безопасному применению опиоидов, обсуждает сложные вопросы лечения в конце жизни без потери уважения к пожеланиям пациента.
Стадии и степени саркомы мягких тканей
Стадия означает, насколько велика опухоль, и распространилась ли она на другие ткани. Степень означает, насколько ненормально раковые клетки выглядят под микроскопом. Онкологи используют стадию и степень саркомы, чтобы выбрать правильную тактику лечения. Оценка степени саркомы основана на 3 факторах:
- дифференциация
- количество митозов
- некроз.
Дифференцировка означает, насколько по-разному клетки саркомы выглядят под микроскопом по сравнению с нормальными клетками.
- Оценка 1 означает, что раковые клетки похожи на нормальные клетки.
- Оценка 2 означает, что раковые клетки выглядят умеренно иначе, чем нормальные клетки.
- Оценка 3 означает, что раковые клетки являются аномальными и сильно отличаются от нормальных клеток.
Митотический счет оценивает, сколько клеток делится под микроскопом.
- 1 балл означает, что делящихся клеток меньше 10.
- 2 балла означают, что делящихся клеток больше 10, но меньше 20.
- Оценка 3 означает, что делящихся клеток больше 20.
Некроз описывает, какая часть саркомы состоит из умирающей ткани.
- 0 означает, что отмершей ткани нет.
- 1 означает, что менее половины (50%) рака составляет отмирающая ткань.
- 2 означает, что более половины (50%) рака составляет отмирающая ткань.
Баллы за дифференцировку, число митозов и некроз складываются для получения степени.
- Степень 1 означает общий балл 2 или 3.
- Степень 2 означает общую оценку 4 или 5.
- Степень 3 означает общую сумму баллов 6,7 или 8.
Онколог может описать саркому как саркому низкой степени (степень 1) или высокой степени (степень 2 или 3). Рак низкой степени злокачественности, вероятно, будет расти медленнее и с меньшей вероятностью распространится на другие части тела. Рак высокой степени злокачественности, вероятно, будет расти быстрее и с большей вероятностью распространиться, чем саркома низкой степени злокачественности.
Двумя основными способами стадирования саркомы являются система TNM и системы счисления. TNM расшифровывается как опухоль, узел, метастаз. Опухоль (Т) и количество стадий зависят от того, в какой части тела находится саркома. Стадия для узла (N) и метастазов (M) одинакова, где бы ни находилась саркома в организме.
Стадии TNM саркомы рук, ног или туловища
Опухоль (Т)
T описывает размер саркомы (области рака).
Выделяют 4 основных стадии Т:
- T1 означает, что опухоль меньше 5 см.
- T2 означает, что рак больше 5 см, но не больше 10 см.
- T3 означает, что рак больше 10 см, но не больше 15 см.
- T4 означает, что опухоль больше 15 см.
Узел (N)
N0 означает одно из следующего:
- в лимфатических узлах нет раковых клеток
- тесты не могут показать, есть ли раковые клетки в лимфатических узлах.
N1 означает наличие раковых клеток как минимум в 1 лимфатическом узле.
Метастаз (М)
- Есть 2 основных этапа - M0 и M1.
- M0 означает, что рак не распространился на другие части тела.
- M1 означает, что рак распространился на другие части тела, такие как легкие.
Количественная система стадирования
В этой системе 4 основных степеней.
Степень 1
- 1а означает, что рак меньше 5 см и не распространился на лимфатические узлы или другие части тела. Раковые клетки имеют степень 1 или не могут быть оценены.
- 1b означает, что рак больше 5 см и не распространился на лимфатические узлы или другие части тела. Раковые клетки имеют степень 1 или не могут быть оценены.
Степень 2
Рак меньше 5 см и не распространился на лимфатические узлы или другие части тела. Раковые клетки имеют степень 2 или 3.
Степень 3
- 3а означает, что опухоль имеет размер от 5 до 10 см и не распространилась на лимфатические узлы или другие части тела. Раковые клетки имеют степень 2 или 3.
- 3b означает, что рак больше 10 см и не распространился на лимфатические узлы или другие части тела. Раковые клетки имеют степень 2 или 3.
Степень 4
Стадия 4 означает, что рак прогрессирует:
- рак распространился на лимфатические узлы, но не на другие части тела
- рак распространился на другие части тела, такие как легкие и лимфатические узлы, которые могут содержать или не содержать раковые клетки.
Выживаемость при всех стадиях и типах сарком мягких тканей
- 75 из 100 человек выживают в течение 1 года и более после постановки диагноза.
- почти 55 из 100 человек выживают в течение 5 и более лет после постановки диагноза
- 45 из 100 человек выживают в течение 10 и более лет после постановки диагноза.
Лечение
Перед началом программы онколечения важно собрать медицинскую документацию, список принимаемых препаратов, в том числе безрецептурных средств и БАДов, и предоставить данную информацию онкологу. Рекомендуется заранее обсудить с командой лечение сопутствующих заболеваний, отказаться от курения и значительного употребления алкоголя, обратить внимание на питание и режим сна. Женщинам детородного возраста необходимо проговорить вопросы контрацепции и планирования беременности, а всем пациентам – сообщить о наличии кардиостимуляторов, металлоконструкций, имплантов, которые могут повлиять на выбор методов визуализации и лучевой терапии. Любые симптомы, вызывающие тревогу, лучше заранее описать специалисту, чтобы учесть их при планировании обследований.
Онкотерапия липосаркомы
Хирургическое лечение липосаркомы направлено на радикальное удаление опухоли с широкой фасциальной или мышечной манжетой, особенно при ретроперитонеальной локализации и высокозлокачественных подвидах. При поражении конечностей стремятся сохранить функцию, но не в ущерб онкологическим принципам; при локализации в забрюшинном пространстве нередко выполняются комбинированные резекции соседних органов. Чистота краёв контролируется патоморфологически.
Лучевая терапия нередко добавляется к операции при липосаркомах конечностей и туловища, если узел крупный, расположен глубоко или края резекции минимальны. Дооперационный вариант позволяет уменьшить объём опухолевой массы и облегчить вмешательство, послеоперационный усиливает контроль в зоне удаления. Выбор режима зависит от локализации, состояния кожи и планируемой реконструкции, используется конформное планирование дозы.
Системная химиотерапия применяется при дедифференцированных, плеоморфных и других агрессивных формах липосарком, а также при метастатическом процессе. В первой линии обычно используются антрациклины, при необходимости добавляется ифосфамид; при прогрессировании рассматриваются трабектедин, эребулин и отдельные таргетные средства в зависимости от молекулярных особенностей. При ограниченных метастазах в лёгких и печени возможны резекции и стереотаксическое облучение в комбинации с лекарственным лечением.
Онкотерапия лейомиосаркомы
Хирургическое лечение лейомиосаркомы предполагает широкое иссечение узла с контролем краёв, причём при ретроперитонеальной локализации и поражении матки планируются сложные комбинированные вмешательства. Для образования в матке часто выполняется гистерэктомия с придатками, для забрюшинных форм — резекция вместе с прилежащими структурами при необходимости. Полнота удаления существенно влияет на частоту местных рецидивов.
Лучевая терапия при лейомиосаркоме используется для усиления локального контроля в зоне операции, особенно при глубоком расположении очага, крупных размерах и сомнительных краях резекции. В случае поражения матки или мягких тканей конечностей выбираются конформные режимы, которые позволяют охватить ложе опухоли при приемлемой нагрузке на соседние органы. При ретроперитонеальных формах лучевое воздействие планируется с особой осторожностью из-за чувствительности кишечника и других структур.
Системная терапия основывается на антрациклинсодержащих схемах, к которым по показаниям добавляется ифосфамид или другие цитостатики, а при прогрессировании используются препараты второй линии, включая трабектедин и пазопаниб. Лейомиосаркома часто проявляет склонность к метастазированию в лёгкие и печень, поэтому лекарственное лечение становится важной частью стратегии. При единичных метастазах возможны локальные вмешательства, в том числе резекции и стереотаксическое облучение в сочетании с системной терапией.
Онкотерапия рабдомиосаркомы
Индукционная химиотерапия при рабдомиосаркоме у детей и взрослых является стартовым этапом и строится на комбинациях винка-алкалоидов, антрациклинов, алкилирующих средств и, при определённых формах, препаратов платины. Целью служит уменьшение объёма первичного очага, контроль микрометастазов и создание условий для органосохраняющего локального вмешательства. Длительность индукционного этапа и состав схем зависят от группы риска.
Хирургический этап направлен на максимально полное удаление опухоли с сохранением функции органа, особенно при локализации в области головы, шеи, мочеполовой системы и конечностей. Операция планируется по данным МРТ и КТ с учётом ответа на химиотерапию; при невозможности радикального вмешательства или угрозе тяжёлых функциональных потерь объём может быть уменьшен, а локальный контроль обеспечивается добавлением лучевой терапии. Патоморфологическая оценка степени некроза позволяет уточнить прогноз.
Лучевая терапия при рабдомиосаркоме играет ключевую роль в контроле остаточной болезни и микроскопического поражения даже при полном удалении узла по данным осмотра. Зоны высокого риска и ложе опухоли облучаются по тщательно рассчитанным планам с учётом возраста, локализации, сопутствующих заболеваний и предыдущей химиотерапии. Современные методики позволяют снизить дозу на критические структуры и одновременно поддерживать достаточную нагрузку на опухолевую зону.
Высокоинтенсивные и высокодозные схемы с поддержкой стволовых клеток рассматриваются при неблагоприятных формах, массивном метастатическом процессе и рецидивах, когда стандартные протоколы уже исчерпаны. Проводится мобилизация стволовых клеток, их забор, затем вводятся высокие дозы цитостатиков и через короткий интервал реинфузируются сохранённые клетки кроветворения. Подобная стратегия повышает противоопухолевый эффект, но требует тщательного отбора пациента.
Онкотерапия синовиальной саркомы
Хирургическое лечение синовиальной саркомы конечностей и туловища предполагает широкое иссечение очага с сохранением конечности там, где удаётся выдержать онкологические критерии. При неблагоприятном соотношении между размером опухоли и возможностью сохранить функцию обсуждается ампутация или экзартикуляция, особенно при множественных рецидивах. Контроль краёв резекции и полноценная реконструкция имеют принципиальное значение.
Лучевая терапия используется у большинства пациентов с синовиальной саркомой при глубоком расположении, крупных размерах и близости критических структур. Дооперационный подход позволяет уменьшить объём опухолевой массы и облегчить резекцию, послеоперационный усиливает контроль в ложе и по ходу фасциальных футляров. Выбор варианта зависит от состояния мягких тканей, предполагаемой раневой поверхности и необходимости сложной пластики.
Системная химиотерапия рекомендована при высоком риске метастазов, метастатическом процессе и рецидивах, основой служат антрациклины в комбинации с ифосфамидом. При ответе на лечение может рассматриваться локальное воздействие на отдельные метастазы в лёгких и других органах, включая резекции и стереотаксическое облучение. В отдельных случаях обсуждаются таргетные и иммуноонкологические режимы в рамках клинических исследований.
Лечение злокачественный опухолей оболочек периферических нервов
Хирургическое лечение MPNST строится на радикальном иссечении опухоли с максимально широкими краями, что нередко требует резекции целого нервного ствола и последующей реконструкции или функционального протезирования конечности. При локализации в области крупных нервных сплетений операции отличаются высокой технической сложностью и планируются с участием нейрохирургов и ортопедов. Особое внимание уделяется пациентам с нейрофиброматозом, у которых риск рецидива повышен.
Лучевая терапия при MPNST используется для снижения вероятности местного рецидива, особенно при крупных, глубоко расположенных опухолях и сомнительных краях резекции. Дооперационный вариант позволяет уменьшить объём опухоли и улучшить условия вмешательства, послеоперационный формирует дополнительный барьер в зоне удаления. При выборе режима учитываются близость спинного мозга, крупных нервных стволов и сосудов, для чего применяется конформное планирование.
Системная химиотерапия назначается при высокой степени злокачественности, множественных рецидивах и метастазах, а также у пациентов с отягощающими факторами риска. Наиболее часто применяются антрациклины в комбинации с ифосфамидом, далее рассматриваются протоколы второй линии. Чувствительность MPNST к цитостатикам варьирует, поэтому динамика оценивается регулярно и при отсутствии эффекта проводится смена подхода.
Онкотерапия фибросаркомы
Хирургическое лечение фибросаркомы мягких тканей основано на широком иссечении опухоли с фасциальной и, при необходимости, мышечной манжетой. Для поражения конечностей планируются органосохраняющие вмешательства при условии соблюдения краёв, при локализации в забрюшинном пространстве нередко выполняются комбинированные резекции. Контроль краёв резекции снижает вероятность местных возвратов.
Лучевая терапия при фибросаркоме усиливает локальный контроль, особенно при больших размерах, глубоком расположении и минимальном краевом отступе. Дооперационный вариант помогает уменьшить объём узла, послеоперационный обрабатывает ложе с учётом фактического расположения рубца и возможных микроскопических остаточных клеток. Используются конформные методики с ограничением дозы на кость, нервно-сосудистые структуры и соседние органы.
Системная химиотерапия показана при высокозлокачественных формах, метастатическом процессе и рецидивах, где риск дальнейшего распространения значителен. Применяются антрациклиновые и ифосфамидсодержащие схемы, а при прогрессировании выбираются режимы второй линии, подбираемые индивидуально. При одиночных метастазах рассматриваются локальные методы контроля, включая резекции и стереотаксическое облучение в комбинации с лекарственной терапией.
Онкотерапия миксофибросаркомы
Хирургическое лечение миксофибросаркомы направлено на максимально широкое иссечение очага, поскольку для данной формы характерна выраженная склонность к местным рецидивам. Операция планируется с учётом глубины расположения, вовлечения фасций и мышц, а при необходимости выполняются повторные расширенные резекции в случае выявления опухолевых клеток по краю. Патоморфологический контроль имеет решающее значение.
Лучевая терапия при миксофибросаркоме применяется при глубоких и крупных образованиях, сомнительных краях резекции и невозможности соблюсти рекомендуемый отступ. Облучается ложе опухоли и зона по ходу фасциальных футляров, где сохраняется риск микроскопического поражения. Использование конформного планирования позволяет удерживать дозу в пределах, безопасных для костей, нервов и суставов.
Системная терапия рассматривается при высокой степени злокачественности, множественных рецидивах и метастатическом процессе. Обычно используются антрациклины, к которым по показаниям добавляется ифосфамид, а при прогрессировании подбираются режимы второй линии. При ограниченных метастазах возможны локальные вмешательства, включая резекции и стереотаксическое облучение отдельных очагов.
Лечение эпителиоидной саркомы
Хирургическое лечение эпителиоидной саркомы требует широкого иссечения поражённой области, часто в дистальных отделах конечностей, где анатомические и функциональные ограничения затрудняют радикальность. При множественных рецидивах и крупных узлах может обсуждаться ампутация сегмента для достижения контроля над процессом. Оценка краёв резекции и вовлечения лимфоузлов имеет большое значение.
Лучевая терапия при эпителиоидной саркоме используется при глубоком расположении, сомнительных краях резекции и поражении регионарных лимфоузлов. Облучается ложе опухоли и зоны регионарного лимфооттока, что снижает риск местных и регионарных возвратов. Выбор дозы и полей согласуется с хирургами и патоморфологами, учитывается объём выполненной лимфодиссекции.
Системная терапия показана при генерализованном процессе, быстром рецидивировании и невозможности радикального локального контроля. Применяются антрациклинсодержащие схемы, к которым могут добавляться ифосфамид и другие цитостатики, а для INI1-негативных опухолей рассматриваются таргетные препараты, например ингибиторы EZH2. Участие в клинических исследованиях часто становится важной возможностью для пациентов данной группы.
Лечение светлоклеточной саркомы
Хирургическое лечение светлоклеточной саркомы сухожильных влагалищ и апоневрозов направлено на широкое иссечение очага с сохранением функциональных структур по возможности. Нередко приходится резецировать участки сухожилий и фасций, чтобы обеспечить адекватный краевой отступ и снизить риск рецидива. При поражении стопы и кисти планирование вмешательства требует тщательного обсуждения между онкохирургом и ортопедом.
Лучевая терапия используется при крупных и глубоких образованиях, сомнительных краях резекции и невозможности достижения радикальности. Облучение ложа опухоли и зон по ходу сухожильных футляров помогает контролировать микроскопическое распространение. Современные методики позволяют ограничить дозу для кожи, сухожилий и суставов, имеющих низкий радиорезерв.
Системная терапия применяется при метастатическом процессе и множественных рецидивах, хотя чувствительность светлоклеточной саркомы к стандартным цитостатикам часто ограничена. Используются антрациклинсодержащие схемы, при прогрессировании рассматриваются экспериментальные таргетные и иммуноонкологические варианты на основании молекулярного профиля. При единичных метастазах, особенно в лёгких, обсуждается метастазэктомия и стереотаксическое облучение.
Онкотерапия альвеолярной саркомы мягких тканей
Хирургическое лечение альвеолярной саркомы мягких тканей основано на широком иссечении узла с максимальным сохранением функции конечности или органа при строгом соблюдении краёв. Опухоль нередко имеет небольшие размеры при выявлении, однако рано даёт метастазы, поэтому тщательная оценка краевого отступа обязательна. При труднодоступной локализации привлекаются дополнительные специалисты.
Лучевая терапия используется при глубоких и крупных очагах, сомнительных краях резекции и в ситуациях, когда радикальное вмешательство невозможно без существенной функциональной потери. Облучение ложа опухоли и близлежащих фасциальных пространств снижает риск местного рецидива. Подбор доз и полей проводится с учётом соседних нервов, сосудов и суставов.
Системная терапия при альвеолярной саркоме часто имеет ограниченную эффективность, поэтому большое значение приобретают таргетные и антиангиогенные подходы, а также иммуноонкологические комбинации при генерализованном процессе. С ранних этапов рассматривается участие в клинических исследованиях, поскольку число стандартных высокоэффективных режимов невелико. При ограниченных метастазах возможна резекция и стереотаксическое облучение.
Лечение дерматофибросаркомы
Хирургическое лечение дерматофибросаркомы протуберанс строится на очень широком иссечении поражённой кожи и подлежащих тканей с большим краевым отступом, часто до фасции и глубже. В качестве альтернативы может использоваться микрографическая хирургия Мооса, при которой удаление проводится послойно с немедленным морфологическим контролем. Задачей служит минимизация риска рецидива при максимально возможном сохранении здоровых тканей.
Лучевая терапия применяется при положительных или минимальных краях резекции, а также в ситуациях, когда по анатомическим причинам невозможно обеспечить достаточный отступ. Облучение ложа опухоли с запасом по периферии помогает компенсировать ограничения хирургического подхода. Используются режимы, адаптированные к локализации, чтобы снизить риск поздних кожных и подкожных осложнений.
Таргетная терапия имеет особое значение при генерализованной дерматофибросаркоме протуберанс и рецидивах с подтверждённой транслокацией COL1A1–PDGFB. Ингибиторы тирозинкиназ, например иматиниб, способны уменьшать опухолевую массу, облегчая последующие операции или стабилизируя болезнь при нерезектабельности. Лечение подбирается по результатам молекулярных исследований и контролируется по данным визуализирующих методов.
Лечение плеоморфной саркомы
Хирургическое лечение недифференцированной плеоморфной саркомы мягких тканей основано на широком иссечении первичного очага с фасциальной и мышечной манжетой, что снижает вероятность локального рецидива. В зависимости от локализации выполняются органосохраняющие операции на конечностях, стенке туловища или в забрюшинном пространстве; при поражении критических структур обсуждается более радикальный объём. Контроль краёв резекции имеет ключевое значение для прогноза.
Лучевая терапия при данной форме саркомы мягких тканей применяется до операции для уменьшения объёма опухоли либо после вмешательства для санации зоны потенциального микроскопического поражения. При предоперационном подходе удаётся сохранить больше функциональных тканей, но возрастает риск послеоперационных осложнений; при послеоперационном облучении дозы распределяются по данным гистологии и топометрии. Используются современные конформные методики, чтобы защитить нервы, сосуды и близлежащие органы.
Системная химиотерапия назначается пациентам с высокозлокачественными, крупными, глубоко расположенными очагами, а также при рецидивах и метастазах. Основу составляют схемы на базе антрациклинов, к которым добавляется ифосфамид или другие цитостатики, далее при прогрессировании рассматриваются препараты второй линии. При ограниченных метастазах в лёгких и других органах возможны локальные вмешательства в сочетании с лекарственной терапией, формируя индивидуальный комбинированный план.
Лечение десмопластической мелкокруглоклеточной опухоли
Индукционная химиотерапия при десмопластической мелкокруглоклеточной опухоли брюшины и других локализаций строится на интенсивных многокомпонентных схемах с антрациклинами, алкилирующими средствами, препаратами платины и винка-алкалоидов. Целью служит уменьшение объёма опухолевой массы и частичная санация микроскопического поражения брюшины. После нескольких циклов оценивается ответ по КТ, МРТ и ПЭТ-КТ.
Циторедуктивная хирургия направлена на максимально полное удаление всех видимых очагов в брюшной полости, на диафрагмальных куполах, в тазу и других зонах. Операция часто включает резекции сальника, участков кишечника, брюшины, отдельных органов; тщательный осмотр брюшной полости помогает выявить дополнительные импланты. Радикальность циторедукции напрямую связана с прогнозом.
Гипертермическая внутрибрюшинная химиотерапия рассматривается в специализированных центрах как дополнение к циторедукции. После удаления видимых очагов в брюшную полость на ограниченное время вводятся растворы цитостатиков, нагретые до контролируемой температуры, что усиливает проникновение препаратов в поверхностные слои тканей и повышает противоопухолевый эффект.
Лучевая терапия может использоваться на зону максимальной опухолевой массы либо на области высокого риска рецидива, особенно при невозможности полноценной циторедукции. Дозы и поля подбираются с учётом чувствительности кишечника и других органов. При генерализованном процессе рассматриваются усиленные схемы системной терапии, высокодозные варианты с поддержкой стволовых клеток и участие в клинических исследованиях.
Лечение солитарной фиброзной опухоли
Хирургическое лечение солитарной фиброзной опухоли, включая варианты с признаками злокачественности, предполагает радикальное иссечение узла с адекватным краевым отступом. При локализации в плевральной полости, забрюшинном пространстве и других сложных областях нередко выполняются комбинированные операции с участием торакальных и абдоминальных хирургов. Объём вмешательства планируется на основании КТ и МРТ.
Лучевая терапия рассматривается при злокачественных вариантах и сомнительных краях резекции, а также при локализации, где риск рецидива высок из-за сложного анатомического строения. Облучение ложа опухоли и прилежащих структур позволяет снизить вероятность местного возврата. Используются конформные методики, направленные на защиту жизненно важных органов грудной и брюшной полости.
Системная терапия при солитарной фиброзной опухоли применяется при метастатическом течении либо при выраженной злокачественной трансформации. Используются антрациклины, антиангиогенные и таргетные препараты, режимы подбираются в зависимости от клинической картины и сопутствующей патологии. При единичных метастазах возможны локальные вмешательства, включая резекции и стереотаксическое облучение отдельных узлов.
Осложнения
Во время онколечения часто отмечаются утомляемость, снижение аппетита, умеренная боль в зоне операции или облучения, локальное покраснение кожи, лёгкое расстройство стула или тошнота, о таких проявлениях пациент заранее предупреждается. Срочное обращение необходимо при подъёме температуры выше пороговых значений, выраженной одышке, нарастающей слабости до невозможности выполнять обычные действия, неконтролируемой боли, свежем кровотечении, многократной рвоте, резкой отёчности конечности, судорогах или нарушении сознания. При появлении подобных признаков важно не ждать очередного приёма, а немедленно связаться с лечащим онкологом либо вызвать неотложную помощь по рекомендованному алгоритму.
Поддержка при боли и дискомфорте в зоне облучения при объёмных мягкотканных саркомах строится на ступенчатой анальгезии с использованием ненаркотических анальгетиков, опиоидов и адъювантных средств при нейропатическом компоненте, дополнительно применяются локальные методы в виде охлаждающих гелей, кремов с анестетиком, аккуратных сухих повязок. По показаниям назначаются регионарные блокады, корректируется режим нагрузок на конечность, подбираются ортезы или костыли, чтобы уменьшить давление на облучённый костный сегмент и снизить риск патологического перелома. При выраженной боли пациент получает разъяснения о цели лучевой терапии, о сроках ожидаемого обезболивающего эффекта, совместно с онкологом подбирается режим приёма анальгетиков не “по требованию”, а по расписанию, что снижает колебания интенсивности симптомов.
Уход за кожей и профилактика лучевых реакций в зоне облучения мягкотканных сарком, дерматофибросаркомы протуберанс, саркомы Капоши и солитарной фиброзной опухоли включает ежедневное бережное очищение без грубых мочалок, использование мягких моющих средств без спирта и запаха, аккуратное промакивание кожи полотенцем. На стадии покраснения применяются специализированные дерматологические кремы и эмоленты, согласованные с радиотерапевтом, исключаются согревающие компрессы, травмирующая одежда, тесное бельё, интенсивное трение. Пациент информируется о недопустимости самостоятельного использования йодных сеток, зелёнки, спиртовых растворов на облучённую область и предупреждается, что любые пузыри, трещины, мокнутие должны сразу обсуждаться с лечащим специалистом.
Профилактика отёка, лимфедемы и контрактур после комбинированного лечения с лучевой терапией при синовиальной саркоме, липосаркоме, фибросаркоме и других саркомах конечностей опирается на раннее подключение реабилитации, обучение щадящим движениям и правильному положению конечности. Реабилитолог подбирает комплекс упражнений для мягкой разработки суставов, растяжения тканей вокруг рубца и облучённой зоны, следит за тем, чтобы нагрузка на мышечно-сухожильный аппарат нарастала постепенно. При склонности к отёкам рекомендуются компрессионный трикотаж, осторожный лимфодренажный массаж, контроль массы тела и ограничение длительного статического положения, особенно стоя или сидя без опоры для конечности.
Нутритивная поддержка направлена на предупреждение снижения массы тела, дефицита белка и витаминов. Диетолог или онколог даёт рекомендации по частому дробному питанию, подбору легкоусвояемых белковых продуктов, дополнительным смесям при снижении аппетита, при необходимости обсуждаются энтеральные или парентеральные методы восполнения. При облучении области живота контролируются тошнота, метеоризм, расстройства стула, по показаниям добавляются противорвотные препараты, средства для коррекции перистальтики и ферментные препараты, а также разъясняется, какие продукты лучше временно ограничить, чтобы уменьшить раздражение кишечника.
Контроль кроветворения и профилактика инфекций у онкопациентов основан на регулярном анализе крови, оценке уровня лейкоцитов, тромбоцитов, гемоглобина. При нейтропении обсуждается необходимость факторов роста и временной коррекции схем сопутствующей системной терапии, при анемии рассматривается эритроцитарная трансфузия или препараты железа. Отдельное внимание уделяется гигиене полости рта, уходу за кожей и ногтями, профилактике грибковых и бактериальных осложнений, пациент получает чёткий список тревожных симптомов (лихорадка, резкое ухудшение самочувствия), при которых нужно немедленно связаться с медицинской командой.
Психологическая помощь учитывает страх инвалидизации, хронической боли, возможной ампутации или крупной реконструктивной операции, а также длительность комбинированного лечения с лучевой терапией. Психолог или психоонколог помогает пациенту сформулировать реальные ожидания от лечения, обсудить страх рецидива, научиться справляться с тревогой и нарушениями сна, при необходимости подключается медикаментозная поддержка с мягкими анксиолитиками или антидепрессантами. Большое значение имеет работа с родственниками, объяснение им особенностей поведения и самочувствия больного, чтобы уменьшить давление и чувство вины, а также использование групп поддержки, где пациенты с саркомами могут обсуждать общий опыт.
Профилактика тромбоэмболических осложнений и поддержка безопасной физической активности основывается на оценке индивидуального риска и подборе стратегии. По показаниям назначаются антикоагулянты в профилактических дозах, пациент обучается простым упражнениям для стоп, голеней, дыхательной гимнастике, периодическому вставанию и ходьбе, если состояние позволяет. Дополнительно обсуждаются отказ от курения, контроль артериального давления, лечение сопутствующих заболеваний сердца и сосудов, что уменьшает суммарный риск осложнений на фоне лучевой терапии и системного лечения сарком.
Список научной литературы:
- Алиев М.Д. Выбор метода реконструкции дефектов у пациентов с местно-распространенными опухолями костей, кожи и мягких тканей нижних конечностей / М.Д. Алиев, В.А. Соболевский, Р.Б. Азимова // Саркомы костей, мягких тканей и опухоли кожи. - 2012. - № 1. - С. 3-14.
- Деньгина Н.В. Возможности современной лучевой терапии в лечении сарком мягких тканей / Н.В. Деньгина, А.В. Жинов // Практическая онкология. - 2013. -Т. 14, № 2. - С. 101-111.
- Курпешев О.К. Результаты химио- и термолучевой терапии больных с саркомой мягких тканей, подвергшихся и не подвергшихся оперативному вмешательству / О.К. Курпешев, А.Л. Зубарев // Онкология. - 2006. - Т. 8, № 3. - С. 255-259.
- Thrall DE, Gillette EL. Soft-tissue sarcomas. Semin Vet Med Surg Small Anim. 1995 Aug;10(3):173-9. PMID: 8532973.
- Cormier JN, Pollock RE. Soft tissue sarcomas. CA Cancer J Clin. 2004 Mar-Apr;54(2):94-109. doi: 10.3322/canjclin.54.2.94. PMID: 15061599.
- Brownstein JM, DeLaney TF. Malignant Soft-Tissue Sarcomas. Hematol Oncol Clin North Am. 2020 Feb;34(1):161-175. doi: 10.1016/j.hoc.2019.08.022. Epub 2019 Oct 28. PMID: 31739942.
- Нуднова Н.В. МР-томографическая диагностика опухолей мягких тканей/ Н.В. Нуднова, Н.В.Кошелева, Е.В. Ганова // Вестн.рентгенологии и радиологии. - 1999. - №6. - С. 35-38.
- Федорова И.В. Комплексная ультразвуковая диагностика опухолей мягких тканей: Автореф.дис. канд.мед.наук: 14.02.13/ И.В. Федорова. -Томск, 2005. - 22 с.
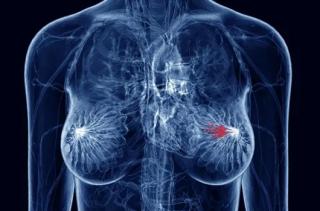
Что надо сделать для ранней диагностики ангиосаркомы молочных желез? Пациенту, в первую очередь, необходимо записаться на консультацию к маммологу. У некоторых женщин рак обнаруживается во время обследования молочных желез с помощью УЗИ молочных желез или маммографии. Для дифференциальной диагностики опухоли дополнительно применяются: биопсия ткани груди МРТ молочных желез с контрастированием.
Что надо сделать для ранней диагностики ангиосаркомы молочных желез? Пациенту, в первую очередь, необходимо записаться на консультацию к маммологу. У некоторых женщин рак обнаруживается во время обследования молочных желез с помощью УЗИ молочных желез или маммографии. Для дифференциальной диагностики опухоли дополнительно применяются: биопсия ткани груди МРТ молочных желез с контрастированием.
Что надо сделать для ранней диагностики рака лимфоузлов? Пациенту, в первую очередь, необходимо записаться на консультацию к хирургу и сделать УЗИ лимфоузлов. После первичного приема врач может назначить дополнительные обследования: Консультацию онколога МРТ лимфоузлов с контрастом.
Что надо сделать для ранней диагностики рака лимфоузлов? Пациенту, в первую очередь, необходимо записаться на консультацию к хирургу и сделать УЗИ лимфоузлов. После первичного приема врач может назначить дополнительные обследования: Консультацию онколога МРТ лимфоузлов с контрастом.
Паническая атака во время МРТ - это частое осложнение, с которым встречаются люди с клаустрофобией. Паническое расстройство - это тревожное расстройство, при котором у вас регулярно случаются внезапные приступы паники или страха. Каждый человек в определенное время испытывает чувство тревоги и паники, это естественная реакция на стрессовые или опасные ситуации.
Паническая атака во время МРТ - это частое осложнение, с которым встречаются люди с клаустрофобией. Паническое расстройство - это тревожное расстройство, при котором у вас регулярно случаются внезапные приступы паники или страха. Каждый человек в определенное время испытывает чувство тревоги и паники, это естественная реакция на стрессовые или опасные ситуации.
 Общегородской центр
Общегородской центр